Αντιδράσεις στις πολυεθνικές εταιρείες φαρμάκων έχει προκαλέσει η πρόταση της Κομισιόν για την αναθεώρηση της φαρμακευτικής πολιτικής και μείωση του χρόνου προστασίας δεδομένων των νέων φαρμάκων κατά δύο χρόνια.
Πιο συγκεκριμένα, η Ευρωπαϊκή Επιτροπή προτείνει μείωση του χρόνου προστασίας δεδομένων κατά δύο χρόνια, από τα περίπου 8 χρόνια από την έγκριση κυκλοφορίας τους, που ισχύει σήμερα, σε 6 χρόνια. Η εξέλιξη αυτή οδηγεί ουσιαστικά σε μείωση της «πατέντας» και δημιουργία γενοσήμων νωρίτερα, σε σχέση με ό,τι συμβαίνει σήμερα.
Το επιχείρημα της Κομισιόν για τη συγκεκριμένη πρόταση είναι η αύξηση του ανταγωνισμού, καθώς με τη μείωση της διάρκειας προστασίας των δεδομένων θα μπουν και άλλες εταιρείες και θα δημιουργηθούν γενόσημα, με αποτέλεσμα να υπάρχει επάρκεια στην αγορά. Πρόκειται για μια «ρηχή» προσέγγιση κατά τους εκπροσώπους των φαρμακευτικών επιχειρήσεων. Όπως εκτιμούν, η μείωση του χρόνου προστασίας θα οδηγήσει σε αυξήσεις τιμών από την πλευρά των εταιρειών, προκειμένου να καλυφθεί η απώλεια εσόδων. Αυτό θα έχει ως αποτέλεσμα υψηλότερες τιμές των καινοτόμων φαρμάκων, που εισάγονται στην αγορά, οι οποίες αυτόματα θα παρασύρουν προς τα πάνω και τις τιμές των γενοσήμων.
Το Ευρωπαϊκό Κοινοβούλιο τον Μάρτιο πρότεινε μια ενδιάμεση λύση, που βρίσκεται πιο κοντά στο ισχύον καθεστώς και προβλέπει συνολικά από 7,5 έως 11,5 χρόνια προστασία δεδομένων. Οι σημερινές προτάσεις αποτυπώνονται στον παρακάτω πίνακα:
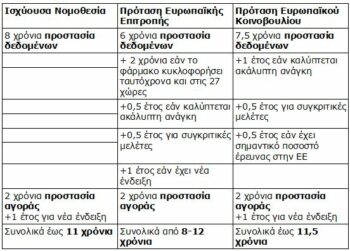
Μελέτες που έχει διενεργήσει ο Σύνδεσμος Φαρμακευτικών Επιχειρήσεων Ελλάδος (ΣΦΕΕ), δείχνουν ότι εάν εφαρμοστεί η πρόταση της Κομισιόν – η ψήφιση της οποίας τοποθετείται χρονικά το 2026 καθώς αναμένεται εκτενής διαβούλευση και από τα κράτη μέλη – η καινοτομία που αναμενόταν τα επόμενα 15 χρόνια θα μειωθεί κατά 22%. Ειδικότερα, 50 από τα 225 φάρμακα δεν θα έρθουν στη χώρα μας. Επιπλέον, σύμφωνα με τις ίδιες μελέτες, δυσκολεύει σημαντικά η πρόσβαση των ασθενών σε καινοτόμες θεραπείες.
Ήδη τα νέα φάρμακα φτάνουν με σημαντική καθυστέρηση στους Έλληνες ασθενείς, σε σύγκριση με άλλους Ευρωπαίους. Στην Ελλάδα το διάστημα 2018-2021 ένα νέο φάρμακο για να μπει στη λεγόμενη Θετική Λίστα, δηλαδή να αποζημιωθεί χρειαζόταν περίπου 674 ημέρες, τη στιγμή που στη Γερμανία ή τη Δανία χρειαζόταν κάτω από 200 ημέρες. Το ίδιο χρονικό διάστημα, πήραν έγκριση από τον Ευρωπαϊκό Οργανισμό Φαρμάκων (ΕΜΑ) 168 φάρμακα, από τα οποία τα 90 ήρθαν στην Ελλάδα. Εξ αυτών μόνο τα 38 με ευρεία πρόσβαση. Τα υπόλοιπα ήταν με περιορισμένη προσβασιμότητα, πχ μέσω ΙΦΕΤ.
Ελλείψεις: Πώς θα βρίσκετε το φάρμακό σας στο app του Υπουργείου Υγείας – Το ελληνικό case study
Ευρώπη: Οκτώ καλές πρακτικές αντιμετώπισης του καρκίνου – Ποιες εφαρμόζει η Ελλάδα
Φαρμακευτική κάνναβη: Τι δείχνει ελληνική έρευνα για τη χορήγησή της σε ογκολογικούς ασθενείς